Một nhóm các nhà nghiên cứu sinh học tại trường Đại học Rice, Hoa Kỳ do kỹ sư sinh học Jeffrey Hartgerink dẫn đầu đã tạo ra một loại vật liệu hydrogel được thiết lập dựa trên các chuỗi peptide có cấu trúc răng cưa để từ đó phát triển phương pháp hiệu quả nhằm phân phối các phân tử thuốc khó tan đến những vị trí chính xác trong cơ thể bệnh nhân. Bài báo về kết quả nghiên cứu được đăng tải trên tạp chí Biomacromolecules của Hiệp hội Hóa học Hoa Kỳ.
Trong những năm gần đây, phòng thí nghiệm của Hartgerink đã cho ra đời nhiều loại vật liệu hydrogel được tạo thành từ các chuỗi peptide tùy chỉnh, đem đến những thay đổi đáng kể trong ứng dụng y khoa bao gồm: phương pháp điều trị nhằm kích thích tăng trưởng các tế bào, phục hồi mô ở người hay liệu pháp điều trị chứng huyết khối cũng như cầm máu trong quá trình phẫu thuật (nhờ sử dụng loại hydrogel với thành phần nọc rắn).
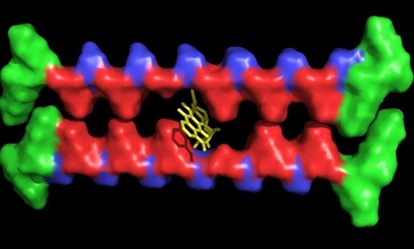
Vật liệu hydrogel mới có dạng sợi nano được tạo thành dựa trên các chuỗi peptide có cấu trúc “răng cưa”. Khoảng cách giữa các răng cưa trong sợi được thiết kế để giữ chân các phân tử thuốc có đặc tính kỵ nước. Loại gel có khả năng phân huỷ sinh học được tiêm để giải phóng những phân tử thuốc dần ra khỏi cơ thể theo thời gian.
Trong nghiên cứu mới, mục tiêu mà kỹ sư Hartgerink cùng hai nghiên cứu sinh trường Rice là I-Che Li và Amanda Moore nhắm tới là xử lý những phân tử thuốc có xu hướng kết thành cục, khó lưu thông trong máu.
Hartgerink cho biết: “Thông thường, các phân tử ưa nước (có khả năng hấp thu nước) có thể được tiêm vào cơ thể người mà không cần thông qua cơ chế phân phối. Các phân tử thuốc có khả năng hòa tan trong nước sẽ di chuyển trong mạch máu và tan ra. Trong khi đó, việc đưa các phân tử thuốc kỵ nước vào trong cơ thể lại là một việc không hề đơn giản. Chính vì vậy, chúng tôi đã đưa chúng vào vị trí khoảng trống giữa các răng cưa trên sợi nano, từ đó, phân tử thuốc được giữ là và theo đó phân phối tới bất cứ vị trí nào được tiêm hydrogel trong cơ thể“.
Điểm khác biệt giữa nghiên cứu mới của Hartgerink và nhiều nghiên cứu được thực hiện trước đó – mà trong đó, các protein hoặc phân tử nhỏ thường bị mắc kẹt trong gel được tạo thành bởi các sợi siêu nhỏ – nằm ở sự thay đổi cấu trúc bên trong sợi. Cụ thể hơn, Hartgerink cùng các cộng sự đã tiến hành loại bỏ một phần cấu trúc bên trong của sợi và gọi đó là cấu trúc răng cưa, đặc biệt đây là môi trường kỵ nước.
Để tạo ra sợi có cấu trúc độc đáo, ban đầu, nhóm nghiên cứu đã thiết lập các chuỗi peptide gồm các axit amin kỵ nước và ưa nước được sắp xếp theo trình tự luân phiên, xen kẽ giữa những khoảng trống răng cưa. Các loại thuốc có phân tử nhỏ kỵ nước sẽ bị hút và mắc kẹt vào những khoảng trống trong quá trình tự lắp ráp để hình thành sợi có cấu trúc răng cưa của các chuỗi peptide.
Hydrogel từ dạng gel biến thành dạng lỏng dưới tác dụng của lực cắt trong quá trình nó di chuyển xuyên qua đầu kim tiêm – hiện tượng này được gọi là hiện tượng thixotropy, sau khi vào bên trong cơ thể, nó lập tức quay trở lại cấu trúc dạng gel ban đầu. Các phân tử thuốc phân bố đan xen trong những khe trống của các peptide cho đến khi được giải phóng khỏi hydrogel. Các chuyên gia cho biết họ đã tiến hành thử nghiệm tiêm hydrogel vào cơ thể bệnh nhân sử dụng các loại thuốc điều trị ung thư, thuốc kháng sinh hay thuốc chống viêm. Bên cạnh đó, họ cũng đang nghiên cứu cách thức giải phóng của phân tử thuốc ra khỏi cơ thể người bệnh theo thời gian.
Hartgerink đánh giá cao cấu trúc “răng cưa” của vật liệu hydrogel mới vì nhờ nó, việc chặn cả các protein ưa nước trong ma trận hydrogel là hoàn toàn khả thi. Ông cho biết: “Mục tiêu mà chúng tôi muốn nhắm tới trong tương lai là sẽ phát triển loại vật liệu có khả năng cùng lúc thực hiện cả hai mục tiêu (giữ chân cả phân tử kỵ nước và ưa nước)“.
P.K.L (NASATI), Theo https://phys.org/news/2016-06-tooth-hydrogels-hard-to-deliver-drugs.html, 7/6/2017