Tập hợp protein, trong đó các protein không khớp được kết hợp lại với nhau để tạo thành các sợi nhỏ, có liên quan đến nhiều bệnh bao gồm Alzheimer, Parkinson và tiểu đường loại II. Mặc dù vai trò chính xác của các sợi này trong các bệnh chưa được hiểu rõ, nhiều phương pháp điều trị hiện tại đối với các bệnh như Alzheimer và Parkinson nhắm vào quá trình tổng hợp. Tuy nhiên, việc tìm ra phác đồ điều trị phù hợp cho những loại thuốc này, có thể gây độc với liều lượng lớn, là một thách thức.
Gần đây, các nhà nghiên cứu từ Trường Kỹ thuật và Khoa học Ứng dụng Harvard (A.AS) của Harvard đã phát triển một mô hình để hiểu rõ hơn về cách thuốc ức chế sự phát triển của protein fibrils, đưa ra hướng dẫn để phát triển các chiến lược hiệu quả hơn để nhắm vào các bệnh tổng hợp protein. Các nhà nghiên cứu phát hiện ra rằng các loại thuốc khác nhau nhắm vào các giai đoạn tổng hợp protein khác nhau và thời gian dùng thuốc đóng vai trò quan trọng trong việc ức chế sự phát triển của fibril.
L Mahadevan, Giáo sư toán học ứng dụng Lola England de Valpine, nói: “Nghiên cứu của chúng tôi nhấn mạnh tầm quan trọng của việc tìm hiểu mối quan hệ giữa động học hóa học của các khối protein không được gấp, cơ chế mà thuốc ức chế sự tổng hợp protein và thời gian quản lý của chúng. Sự hiểu biết này có thể có ý nghĩa quan trọng đối với các giao thức can thiệp để ngăn chặn sự tổng hợp protein bệnh lý”.
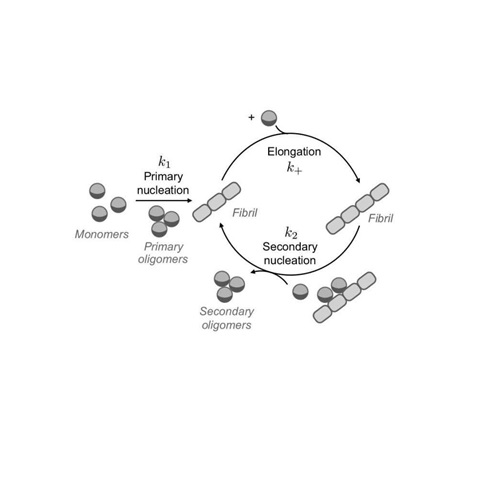
Sự tổng hợp protein bao gồm một số bước, bắt đầu với cái được gọi là tạo mầm đầu tiên, trong đó những đoạn này tích tụ đến 1 số lượng dư thừa và hình thành khối tập hợp các protein không được gấp (misfolded protein) được kết hợp với nhau để tạo thành sợi nhỏ, sau đó kéo dài. Khi một số lượng lớn sợi nhỏ được hình thành, tập hợp sẽ tăng tốc do một quá trình được gọi là tạo mầm thứ cấp, dẫn đến tăng trưởng theo cấp số nhân. Bước đầu tiên liên quan đến sự hình thành của các sợi nhỏ là rất chậm, thường mất vài thập kỷ, điều này có thể giải thích tại sao bệnh Alzheimer thường ảnh hưởng đến những người ở tuổi già. Tuy nhiên, một khi những sợi nhỏ đầu tiên được hình thành, bệnh có thể tiến triển rất nhanh.
Sử dụng các phương pháp toán học từ lý thuyết điều khiển, kết hợp với vật lý tổng hợp protein, các nhà nghiên cứu đã đưa ra dự đoán lý thuyết về cách thức và thời điểm can thiệp sử dụng thuốc. Để kiểm tra kết quả của họ, các nhà nghiên cứu đã xem xét dữ liệu được công bố trước đây về hiệu quả của thuốc trong một sinh vật mẫu, loài giun tròn, C. Elegans, nơi người ta có thể kích hoạt sự hình thành của Amyloid b, một loại
protein không liên quan đến bệnh Alzheimer. Điều trị của nó được thực hiện bằng cách sử dụng hai hợp chất ức chế sự hình thành của Amyloid b: Bexarotene và DesAb29- 35.
Các nhà nghiên cứu phát hiện ra rằng hiệu quả của thuốc phụ thuộc vào việc hợp chất ức chế quá trình tạo mầm nguyên phát hay tạo mầm thứ cấp. Bexarotene, ví dụ, ức chế chọn lọc mầm nguyên phát xảy ra sớm trong bệnh trong khi DesAb29-36 ức chế tạo mầm thứ cấp xảy ra sau đó. Trong trường hợp không có thuốc, tập hợp Amyloid-b gây tê liệt ở giun. Khi Bexarotene được đưa ra khi bắt đầu bệnh ở giai đoạn ấu trùng, dữ liệu được công bố cho thấy có sự phục hồi đáng kể khả năng di chuyển của giun. Dữ liệu cũng cho thấy DesAb29-36 có hiệu quả hơn khi được sử dụng sau này trong quá trình tiến triển của bệnh.
Mahadevan, giải thích: “Bằng cách kết hợp các khái niệm nổi tiếng từ hai lĩnh vực khác nhau, động lực của quá trình tổng hợp protein và lý thuyết điều khiển tối ưu, chúng tôi đã liên kết các hiện tượng ở quy mô phân tử với các chiến lược vĩ mô có liên quan đến một vấn đề thực tế, thực tế”.
Các tác giả tại Havard Thomas CT Michaels, Christoph Weber, cho biết: “Cách tiếp cận của chúng tôi, dựa trên sự hiểu biết chi tiết về quá trình tổng hợp và sử dụng sự hiểu biết này để thiết kế những chiến lược tiềm năng hợp lý. Nó sẽ cho phép mọi người kiểm tra hiệu quả hợp chất khác nhau chống lại sự kết hợp trong điều kiện tối ưu ở mức độ phát hiện thuốc và sàng lọc thuốc. Từ những điều kiện tối ưu này, người ta có thể ngoại suy các điều kiện tối ưu cho một thử nghiệm. Vì vậy, theo nghĩa này, công việc của chúng tôi có thể giúp hạt giống thử nghiệm tiềm năng”.
Nghiên cứu được công bố trong Kỷ yếu của Viện Hàn lâm Khoa học Quốc gia.
N.T.T (NASATI), theo https://medicalxpress.com/news/2019-08-math-alzheimer-
parkinson-diseases.html